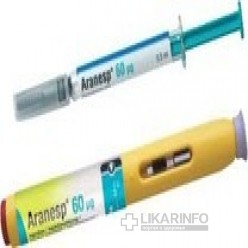
Аранесп
О препарате:
Стимулятор гемопоэза, антианемический препарат.
Показания и дозировка:
Лечение симптоматической анемии у взрослых и детей c хронической почечной недостаточностью
Лечение симптоматической анемии у взрослых пациентов с немиелоидными злокачественными новообразованиями, получающих химиотерапию
Лечение препаратом Аранесп должно проводиться врачами, имеющими опыт назначения по вышеупомянутым показаниям.
Аранесп (SureClick) поставляется готовым для применения в предварительно заполненных шприц-ручках (ПЗШР). ПЗШР предназначаются только для подкожных инъекций. Инструкции по применению препарата, обращению с ним и порядку его уничтожения приводятся в разделе Особые указания по использованию.
Лечение анемии у больных с хронической почечной недостаточностью.
Аранесп можно вводить подкожно или внутривенно. Подкожное введение предпочтительно для больных, не получающих гемодиализ, для предотвращения пункции периферических вен. Целью терапии является повышение содержания гемоглобина до уровня, превышающего 110 г/л. Для каждого пациента необходим индивидуальный подбор требуемого гемоглобина выше 110 г/л. Следует избегать повышения гемоглобина более чем на 20 г/л за 4 недели или гемоглобина выше 140 г/л. Клинические исследования показали, что индивидуальный ответ пациента может быть различным. Тем не менее, на начальных этапах следует придерживаться приведенных ниже рекомендаций, как для взрослых, так и для детей, с последующей оптимизацией терапии в зависимости от клинических показаний.
Лечение препаратом Аранесп включает две стадии- фаза коррекции и поддерживающая фаза:
Фаза коррекции.
Начальная доза при подкожном или внутривенном введении должна составлять 0,45 мкг/кг массы тела при однократном еженедельном введении. Альтернативно, для больных, не получающих диализ, допускается подкожное введение препарата в начальной дозе 0,75 мкг/кг массы тела каждые две недели. Если повышение концентрации гемоглобина оказывается недостаточным (менее 10 г/л за 4 недели), доза препарата увеличивается приблизительно на 25%. Повышение дозы препарата не должно осуществляться чаще, чем один раз в четыре недели.
Если концентрация гемоглобина возрастает более чем на 25 г/л за четыре недели, дозу Аранеспа следует снизить на 25-50% в зависимости от скорости повышения гемоглобина. Если содержание гемоглобина превышает 140 г/л терапию следует прервать до снижения гемоглобина ниже 130 г/л, а затем возобновить введение препарата в дозе, сниженной примерно на 25% относительно предыдущей. Гемоглобин следует измерять еженедельно или раз в две недели до его стабилизации. Впоследствии гемоглобин можно оценивать периодически.
Поддерживающая фаза.
В период поддерживающей фазы можно продолжать однократное еженедельное введение препарата Аранесп или перейти на введение каждые две недели. При переводе пациентов, находящихся на диализе, с еженедельных инъекций на режим введения однократно раз в две недели, исходная доза должна вдвое превышать дозу, вводившуюся один раз в неделю. Для пациентов, не получающих диализа, после достижения требуемой концентрации гемоглобина на фоне назначения препарата раз в две недели, его подкожное введение может производиться один раз в месяц с использованием исходной дозы вдвое превышающей предыдущую дозу, вводившуюся раз в две недели.
Титрование дозы с целью поддержания требуемой концентрации гемоглобина следует производить так часто, как это требуется.
Для каждого пациента необходим индивидуальный подбор требуемого гемоглобина выше 110 г/л. Если для поддержания требуемого гемоглобина необходима оптимизация дозы Аранеспа, ее рекомендуется увеличивать приблизительно на 25%. В случае, если наблюдается повышение гемоглобина более, чем 20 г/л за 4 недели, дозу препарата следует уменьшить приблизительно на 25%, в зависимости от скорости повышения, Если содержание гемоглобина превышает 140 г/л, терапию следует прервать до уменьшения концентрации ниже 130 г/л, а затем возобновить введение препарата в дозе, меньше примерно на 25% относительно предыдущей.
После любого изменения дозы или режима введения, содержание гемоглобина следует контролировать каждую 1 или 2 недели. Изменение дозы во время поддерживающей фазы должно выполняться не чаще одного раза в две недели.
При изменении пути введения препарата следует использовать те же дозы препарата и осуществлять мониторинг концентрации гемоглобина раз в 1-2 недели с целью поддержания требуемого уровня гемоглобина.
Пациентов, получающих еженедельно по одной, две или три инъекции рчЭпо, можно перевести на режим однократного еженедельного введения Аранеспа или его введение один раз в две недели. Исходную еженедельную дозу Аранеспа (мкг/неделю) определяют,разделив общую еженедельную дозу рчЭпо (МЕ/неделю) на 200. Исходную дозу Аранеспа (мкг/ в две недели) при режиме введения один раз в две недели определяют путем деления суммарной кумулятивной дозы рчЭпо, введенного за двухнедельный период, на 200. Ввиду известной индивидуальной вариабельности, для отдельных больных может потребоваться титрование доз до получения оптимального терапевтического эффекта.
При замещении рчЭпо на препарат Аранесп. измерение уровня гемоглобина следует выполнять не реже одного раза в неделю или в две недели, а способ введения препарата должен оставаться неизменным.
Лечение симптоматической анемии у онкологических больных.
Аранесп следует вводить подкожно пациентам с анемией (при концентрации гемоглобина ≤110 г/л.)
Рекомендованная начальная доза составляет 500 мкг (6,75 мкг/кг) при введении раз в три недели. Если клинический ответ через девять недель неадекватен (утомляемость, содержание гемоглобина), дальнейшая терапия может оказаться неэффективной.
Альтернативно, один раз в неделю препарат можно вводить в дозе 2,25 мкг/кг массы тела.
Применение Аранеспа прекращают примерно через четыре недели после завершения химиотерапии.
Содержание гемоглобина не должно превышать 130 г/л.
После достижения целевого гемоглобина дозу препарата следует снизить на 25-50% для поддержания гемоглобина на соответствующем уровне. При необходимости допускается дальнейшее снижение дозы, чтобы не допустить возрастания концентрации гемоглобина более 130 г/л.
Если скорость возрастания гемоглобина превышает 20 г/л в течение 4 недель, дозу препарата следует снизить на 25-50%.
Передозировка:
Аранесп характеризуется широким диапазоном терапевтических доз. Даже при очень высокой концентрации препарата в сыворотке крови, не наблюдалось симптомов передозировки.
Лечение: в случае выявления полицитемии введение Аранеспа следует временно прекратить. При наличии клинических показаний может быть выполнена флеботомия.
Побочные эффекты:
Зарегистрированы сообщения о развитии серьезных аллергических реакций, включающих анафилактические реакции, ангионевротический отек, аллергический бронхоспазм, сыпь и крапивницу, связанных с приемом дарбэпоэтина альфа.
Данные, полученные в контролируемых исследованиях
Пациенты с хронической почечной недостаточностью:
В контролируемых исследованиях из 1357 пациентов, 766 пациентов получали Аранесп и 591 пациент получал рекомбинантный эритропоэтин человека. 83% находились на диализе, 17% - нет.
При п/к введении Аранеспа сообщалось о боли в месте инъекции как связанной с применением препарата и чаще регистрировавшейся в группе дарбэпоэтина, чем в группе, получавшей рекомбинантный эритропоэтин человека. Дискомфорт в месте инъекции, как правило, был незначительным и преходящим, и отмечался, преимущественно, после первой инъекции.
Частота нежелательных реакций, расцененных как связанные с лечением Аранеспом, в контролируемых клинических исследованиях составила:
Со стороны сердечно-сосудистой системы: очень часто (≥1/10) - повышение АД.
Дерматологические реакции: часто (≥1/100, <1/10) - сыпь, эритема.
Со стороны системы кроветворения: редко (≥1/10 000, <1/1000) - тромбоэмболия.
Местные реакции: часто (≥1/100, <1/10) - боль в месте инъекции.
Пациенты с онкологическими заболеваниями:
Нежелательные реакции были определены на основании объединенных данных семи рандомизированных двойных слепых плацебо-контролируемых исследований Аранеспа, включавших 2112 пациентов (Аранесп 1200, плацебо 912). В клинические исследования включались пациенты с солидными опухолями (например, легких, молочной железы, толстой кишки, яичников) и лимфоидными злокачественными новообразованиями (например, лимфомой, множественной миеломой).
Частота нежелательных эффектов, расцененных как связанные с лечением Аранеспом, в контролируемых клинических исследованиях составляет:
Дерматологические реакции: часто (≥1/100, <1/10) - сыпь, эритема.
Со стороны системы кроветворения: редко (≥1/10 000, <1/1000) - тромбоэмболия, включая тромбоэмболию легочной артерии.
Местные реакции: очень часто (≥1/10) - отек; часто (≥1/100, <1/10) - боль в месте инъекции.
Данные пострегистрационного мониторинга безопасности:
Во время применения Аранеспа в клинической практике сообщалось о развитии следующих нежелательных реакций: парциальная красноклеточная аплазия (в отдельных случаях в связи с терапией Аранеспом сообщалось о нейтрализующих антителах к эритропоэтину, опосредующих парциальную красноклеточную аплазию (ПККА). Главным образом эти общения поступали для пациентов с хронической почечной недостаточностью, получавших препарат п/к. В случае подтверждения диагноза ПККА терапия Аранеспом должна быть прекращена, и пациенты не должны быть переведены на другой рекомбинантный эритропоэтин); аллергические реакции, включая анафилактические реакции, ангионевротический отек, кожную сыпь и крапивницу; судороги.
Противопоказания:
Плохо контролируемая артериальная гипертензия
Повышенная чувствительность к дарбэпоэтину альфа, рчЭпо или любому компоненту препарата
С осторожностью следует применять препарат у пациентов с заболеваниями печени, серповидно-клеточной анемией.
Адекватных и строго контролируемых клинических исследований по безопасности применения препарата при беременности не проводилось. С осторожностью и после тщательной оценки ожидаемой пользы терапии для матери и потенциального риска для плода следует назначать препарат беременным женщинам.
При необходимости назначения препарата в период лактации грудное вскармливание следует прекратить.
В испытаниях, проводившихся на крысах и кроликах, не наблюдалось клинически значимого влияния на беременность,эмбриональное/фетальное развитие, роды или постнатальное развитие. Уровень проникновения препарата через плацентубыл минимальным. Изменений фертильности не отмечалось.
Взаимодействие с другими лекарствами и алкоголем:
Клинические данные, полученные до настоящего времени, не содержат указаний на взаимодействие Аранеспа с другими веществами. Однако известно, что потенциально возможно его взаимодействие с препаратами, характеризующимися высокой степенью сродства к эритроцитам, такими как циклоспорин, такролимус. При одновременном назначении дарбэпоэтина альфа с любыми подобными лекарственными средствами следует контролировать уровень их содержания в сыворотке крови с модификацией дозы в случае повышения концентрации гемоглобина.
Ввиду того, что исследования по совместимости не проводились, препарат Аранесп не следует смешивать или вводить в виде инфузии вместе с другими медицинскими препаратами.
Состав и свойства:
Дарбэпоэтин альфа (рекомбинантный) 25 мкг 10 мкг. Вспомогательные вещества:натрия дигидрофосфата моногидрат, натрия гидрофосфат, натрия хлорид, полисорбат 80, вода д/и.
Дарбэпоэтин альфа (рекомбинантный) 40 мкг 15 мкг. Вспомогательные вещества:натрия дигидрофосфата моногидрат, натрия гидрофосфат, натрия хлорид, полисорбат 80, вода д/и.
Дарбэпоэтин альфа (рекомбинантный) 40 мкг 20 мкг. Вспомогательные вещества:натрия дигидрофосфата моногидрат, натрия гидрофосфат, натрия хлорид, полисорбат 80, вода д/и.
Дарбэпоэтин альфа (рекомбинантный) 100 мкг 30 мкг. Вспомогательные вещества:натрия дигидрофосфата моногидрат, натрия гидрофосфат, натрия хлорид, полисорбат 80, вода д/и.
Дарбэпоэтин альфа (рекомбинантный) 100 мкг 40 мкг. Вспомогательные вещества:натрия дигидрофосфата моногидрат, натрия гидрофосфат, натрия хлорид, полисорбат 80, вода д/и.
Дарбэпоэтин альфа (рекомбинантный) 100 мкг 50 мкг. Вспомогательные вещества:натрия дигидрофосфата моногидрат, натрия гидрофосфат, натрия хлорид, полисорбат 80, вода д/и.
Дарбэпоэтин альфа (рекомбинантный) 200 мкг 60 мкг. Вспомогательные вещества:натрия дигидрофосфата моногидрат, натрия гидрофосфат, натрия хлорид, полисорбат 80, вода д/и.
Дарбэпоэтин альфа (рекомбинантный) 200 мкг 80 мкг. Вспомогательные вещества:натрия дигидрофосфата моногидрат, натрия гидрофосфат, натрия хлорид, полисорбат 80, вода д/и.
Дарбэпоэтин альфа (рекомбинантный) 200 мкг 100 мкг. Вспомогательные вещества:натрия дигидрофосфата моногидрат, натрия гидрофосфат, натрия хлорид, полисорбат 80, вода д/и.
Дарбэпоэтин альфа (рекомбинантный) 500 мкг 150 мкг. Вспомогательные вещества:натрия дигидрофосфата моногидрат, натрия гидрофосфат, натрия хлорид, полисорбат 80, вода д/и.
Дарбэпоэтин альфа (рекомбинантный) 500 мкг 300 мкг. Вспомогательные вещества:натрия дигидрофосфата моногидрат, натрия гидрофосфат, натрия хлорид, полисорбат 80, вода д/и.
Дарбэпоэтин альфа (рекомбинантный) 500 мкг. Вспомогательные вещества:натрия дигидрофосфата моногидрат, натрия гидрофосфат, натрия хлорид, полисорбат 80, вода д/и.
Форма выпуска:
Раствор для инъекций
Фармакологическое действие:
Стимулятор гемопоэза, антианемический препарат. Дарбэпоэтин альфа производится с использованием генной технологии в клетках яичников китайского хомяка (СНО-К1). Стимулирует эритропоэз по тому же механизму, что и эндогенный эритропоэтин. Дарбэпоэтин альфа содержит пять N-связанных углеводных цепей, в то время как эндогенный гормон и рекомбинантные человеческие эритропоэтины (рчЭпо) имеют всего три цепи. Дополнительные остатки сахаров, с молекулярной точки зрения, не отличаются от таковых, представленных в эндогенном гормоне. Вследствие повышенного содержания углеводов дарбэпоэтин альфа обладает более длительным T1/2, по сравнению с рчЭпо, а, следовательно, и большей активностью in vivo. Несмотря на указанные изменения молекулярной структуры дарбэпоэтин альфа сохраняет очень узкую специфичность к эритропоэтиновому рецептору.
Эритропоэтин - фактор роста, который в основном стимулирует образование эритроцитов. Рецепторы к эритропоэтину могут экспрессироваться на поверхности различных опухолевых клеток.
Условия хранения:
Препарат следует хранить в недоступном для детей, защищенном от света месте, при температуре от 2° до 8°С; не замораживать. Срок годности - 2 года.
Перед амбулаторным использованием Аранесп может быть однократно перемещен из места хранения в условия комнатной температуры (до 25°С) на максимальный период 7 дней. Однократно извлеченный из холодильника и достигший комнатной температуры (до 25°С) шприц следует использовать в течение 7 дней или уничтожить.
Общая информация
-
Форма продажи:по рецепту
-
Действующее в-о:Дарбэпоэтин альфа




















Отзывы
Войти Зарегистрироваться